A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou, nesta segunda-feira (6), a prorrogação da dispensa de registro para que o Ministério da Saúde importe e utilize no Brasil o medicamento Tecovirimat, para tratamento da mpox.
A decisão da Diretoria Colegiada (Dicol) aprovou por unanimidade a solicitação de prorrogação feita pela Pasta. A diretora relatora Meiruze Freitas destacou em seu voto que o vírus causador da Mpox ainda persiste em circulação no país, que não há outro medicamento aprovado para o tratamento da mpox e que a decisão mais recente da OMS foi pela manutenção da Emergência de Saúde Pública de Interesse Internacional.
Leia também: Arthur Lira afirma que há vontade política para votar reforma tributária neste ano
A prorrogação da dispensa temporária e excepcional é válida por mais seis meses e se aplica somente ao Ministério da Saúde, desde que não haja revogação expressa pela Anvisa.
No Brasil, até o momento, não há submissão de protocolo de ensaio clínico a ser conduzido nacionalmente para medicamento voltado ao tratamento da mpox. Também não existe protocolo submetido ou mesmo medicamento já registrado pela Anvisa com a indicação de tratamento da doença.
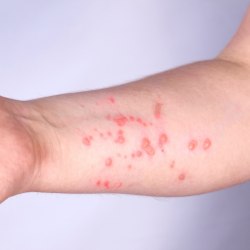
O que é mpox?
Em novembro de 2022, a Organização Mundial de Saúde (OMS) passou a utilizar o termo “mpox” (do inglês monkeypox), para tratar da varíola dos macacos. A mudança veio após a organização receber diversas reclamações sobre o nome da doença, onde diziam ser racista e estigmatizante.
Leia também: Escolas que serviram de abrigo no litoral norte de SP retomam aulas
REDES SOCIAIS